מודל AI מהטכניון מנבא למי תועיל כימותרפיה במאבק בסרטן השד
כלי חדשני שפיתחו חוקרי הטכניון מאמת בניסוי קליני את היכולת לחזות תוך דקות את תגובת המטופלת לטיפול הכימו, על בסיס דגימת רקמה פתולוגית רגילה, מה שינגיש רפואה מותאמת אישית למטופלות
אחת ההחלטות המורכבות ביותר הניצבות בפני אונקולוגים המטפלים בסרטן שד בשלב מוקדם, היא ההכרעה אם להוסיף טיפול כימותרפי לאחר הניתוח. מצד אחד, כימותרפיה עשויה להיות מצילת חיים בהשמדת תאי סרטן שנותרו בגוף ובהפחתת הסיכון לחזרת המחלה; אך מהצד השני, היא גורמת לתופעות לוואי קשות וארוכות טווח ולפגיעה באיכות החיים, ובמקרים רבים בסופו של עניין גם עלולה שלא להועיל למטופלת. לפיכך, אתגר מרכזי הוא לקבוע מראש, כבר בשלב האבחון, מי מהנשים המאובחנות (כ-5,000 בישראל לבדה וכ-2.3 מיליון ברחבי העולם מדי שנה) תפיק תועלת אמיתית מהטיפול – ומי לא. בהיעדר חיזוי מדויק, חלק מהנשים מקבלות כימותרפיה מיותרת ואחרות מפספסות טיפול שיכול היה לסייע להן.
כיום, בדיקות גנומיות, כמו 'אונקוטייפ שד', מסייעות בהערכת הסיכון להישנות המחלה והתועלת הפוטנציאלית מטיפולי כימותרפיה, אך הן יקרות, נמשכות שבועות ואינן נגישות למטופלות רבות בעולם. בנוסף, הדיוק שלהן אינו מושלם, מה שלעתים מוביל להחלטות טיפול שגויות.

חוקרי הטכניון שפיתחו את כלי ה-AI לגילוי התאמת הכימו. מימין לשמאל: פרופ' דביר ארן, ראש המעבדה למדע נתונים ביו רפואי בפקולטה לביולוגיה; ד"ר גיל שמאי, מוביל המחקר מהפקולטה למדעי המחשב; ו-פרופ' רון קימל, ראש המעבדה לעיבוד גיאומטרי של תמונות בפקולטה למדעי המחשב. צילום: דוברות הטכניון ו-ניצן זוהר (בהתאמה)
מאימון על 170 אלף דגימות ועד אימות בניסוי ענק
כעת הדברים עומדים להשתנות – חוקרים מהטכניון, יחד עם עמיתים בארצות הברית ובאירופה, פיתחו מודל בינה מלאכותית המסוגל להעריך הן את הסיכון לחזרת סרטן השד והן את התועלת הצפויה מהכימותרפיה. הכלי החדשני, שאודותיו דווח בכתב העת המדעי The Lancet Oncology ושהוצג בכנס ESMO, עשוי להציע פתרון מדויק, מהיר וזמין יותר לסוגיה. המודל שפותח מסתמך על דגימת רקמה שנלקחת מהגידול ממילא בזמן האבחון הראשוני לשם הבדיקה הפתולוגית.
צוות המחקר, בהובלת ד"ר גיל שמאי ופרופ' רון קימל מהפקולטה למדעי המחשב ע"ש הנרי ומרילין טאוב, בשיתוף פרופ' דביר ארן מהפקולטה לביולוגיה, השתמש במומחיות שנצברה במשך שמונה שנים ובמאגרי מידע גדולים של דגימות פתולוגיה דיגיטליות, שאומנו על יותר מ-170 אלף דגימות.
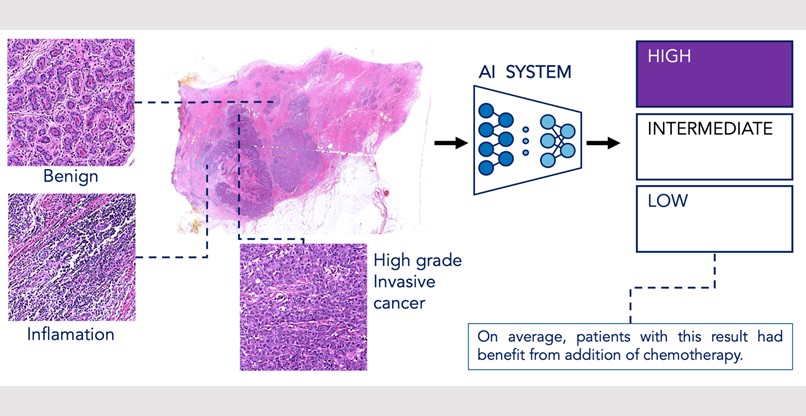
באיור: מערכת ה-AI מפענחת דגימה של רקמת סרטן שד שנסרקה דיגיטלית. המערכת מעריכה את ההסתברות לחזרת המחלה ואת הסבירות לתועלת מטיפול כימותרפי באמצעות ניתוח דפוסים ויזואליים שקשורים להתנהגות הביולוגית של הסרטן, כגון קצב חלוקה של תאים, צורת התאים, מבנה רקמתי המעיד על אגרסיביות וסימנים לתגובה של מערכת החיסון. צילום: דוברות הטכניון
המערכת שפותחה מנתחת תמונה של דגימת הרקמה ברזולוציה גבוהה ומחפשת דפוסים חזותיים זעירים, הקשורים להתנהגות הביולוגית של הסרטן. דפוסים אלה כוללים קצב חלוקת תאים, צורת תאים, מבנה רקמתי המעיד על אגרסיביות וסימנים לתגובת מערכת החיסון, שאינם ניתנים לכימות שיטתי ועקבי על ידי המוח האנושי. פרופ' קימל הסביר כי בדומה לבדיקת צבע עיניים באמצעות התבוננות בהן, במקום בבדיקת גנים, המערכת בוחנת ישירות את תמונת צביעת הרקמה הסרטנית וזאת כדי לחלץ חתימה חזותית המעידה על הטיפול המיטבי פר מטופלת.
על פי הטכניון, המודל אומת במחקר בין-לאומי ובניסוי קליני אקראי רחב היקף, וכן מול נתונים מבתי חולים ברחבי העולם. אימות זה כלל אלפי מטופלות נוספות בבתי חולים באוסטרליה, בארצות הברית ובישראל (המרכז הרפואי כרמל, המרכז הרפואי העמק והמרכז הרפואי שיבא), והראה ביצועים עקביים. החוקרים אף קיבלו גישה ייחודית לנתונים ודגימות קליניות ממחקר TAILORx, שהיה ניסוי אקראי על יותר מעשרת אלפים חולות סרטן שד. הניסוי המסוים איפשר לבחון באופן מהימן את יכולת המודל לנבא תועלת מכימותרפיה, ולא רק להעריך סיכון סטטיסטי להישנות המחלה, כפי שציין ד"ר שמאי.
פרופ' ארן הדגיש כי זהו מודל הבינה המלאכותית הראשון שאומת כיכול לנבא תועלת טיפול כלשהי בסרטן השד, מתוך דגימות פתולוגיות.
הליך מהיר, פשוט וזול בהרבה
יתרון נוסף של הפיתוח הוא שהתהליך הקליני הוא פשוט: דגימת הרקמה נסרקת דיגיטלית ומועברת לפענוח במודל החישובי, ובתוך דקות מתקבל ציון מספרי המסייע לאונקולוגים ולמטופלות לקבל החלטה מדויקת יותר בנוגע לטיפול הכימי. ד"ר שמאי ציין כי למרות שאי אפשר לנסח כללים פשוטים המתארים את מנגנון ההחלטה המדויק של המערכת, החוקרים הצליחו לאמת את נכונות תחזיותיה ועקביותן.
מאחר שהבדיקה אינה מצריכה אבחון גנומי מעבדתי מורכב או דגימה נוספת, היא מהירה וזולה יותר. ניתן לבצע את הבדיקה המדוברת בכל מעבדה פתולוגית עם ציוד בסיסי לסריקת רקמות וכן עם חיבור לאינטרנט. לפיכך, במדינות מתפתחות, שבהן בדיקות גנומיות כמעט אינן קיימות, בדיקה כזו עשויה להרחיב משמעותית את הגישה לרפואה מותאמת אישית, וגם במדינות מערביות היא צפויה לקצר, להוזיל ולדייק את האבחון.
בשלב זה, צוות המחקר מקדם צעדים להטמעת המודל בישראל ופועל במקביל לניסוי קליני בברזיל ובהודו. החוקרים גם פועלים לשיפור דיוק המודל ולהרחבתו לסוגי סרטן נוספים. בהמשך, בכוונת החוקרים להקים חברה שתפתח בדיקות אלו ותהפוך אותן לנגישות, מדויקות ומהירות באופן משמעותי בהשוואה לבדיקות הקיימות כיום.













תגובות
(0)